

《Tumor公社》 肿瘤医学开放式媒体平台,打造肿瘤医学领域一站式解决方案,致力于为用户公众及患者提供及时、全面的肿瘤资讯、科普知识。看百科、找医生、指南分享、搭建医生与患者、患者与患者之间的桥梁,让更多人了解肿瘤、认识肿瘤、助力健康中国2030规划纲要,推动全面科学素质普及,共建肿瘤医学科普生态圈。




专注肿瘤专家报道,专注肿瘤人文报道,全面、细致、详实的让你了解每一位肿瘤领域大咖。

中国抗癌协会早癌筛查科普教育基地官方账号
引用格式 赫捷, 陈万青, 李霓, 等. 中国女性乳腺癌筛查与早诊早治指南(2021,北京)[J]. 中华肿瘤杂志, 2021, 43(4):357-382. DOI:10.3760/cma.j.cn112152-20210119-00061.
中国女性乳腺癌筛查与早诊早治指南(2021,北京)
赫捷1 陈万青1 李霓1 沈洪兵2 李江1 王勇1 李静1 田金徽3 周宝森4
中国女性乳腺癌筛查与早诊早治指南制定顾问组 中国女性乳腺癌筛查与早诊早治指南制定专家组 中国女性乳腺癌筛查与早诊早治指南制定工作组
1国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院 100021;2南京医科大学公共卫生学院 肿瘤个体化医学省部共建协同创新中心 211166;3兰州大学循证医学中心 730000; 4中国医科大学公共卫生学院,沈阳 110122
通信作者:赫捷, 国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院胸外科 100021, Email:hejie@cicams.ac.cn
【摘要】 乳腺癌是中国女性最常见的恶性肿瘤,发病率位居中国女性恶性肿瘤首位。国家癌症中心受国家卫生健康委员会疾病预防控制局委托,根据《世界卫生组织指南制定手册》制定女性乳腺癌筛查与早诊早治指南。制作系统评价流程参考Cochrane协作网的方法,证据质量与推荐强度的分级采用推荐意见分级的评估、制定及评价方法,并根据国际实践指南报告规范条目进行报告。在系统评价结果的基础上,结合中国国情,综合考虑了证据的利弊、证据的质量、筛查经济成本、多学科临床调查对象的反馈和面对面的专家共识意见,针对乳腺癌筛查与早诊早治中适宜人群、技术流程等进行循证推荐,旨在规范女性乳腺癌筛查与早诊早治实践,提升中国女性乳腺癌防控效果。
【主题词】乳腺肿瘤;女性;筛查;早诊早治;指南;中国
DOI:10.3760/cma.j.cn112152-20210119-00061
一、引言
乳腺癌是女性常见的恶性肿瘤,其发病率和死亡率分别位列我国女性恶性肿瘤的第1位和第4位。2015年我国女性乳腺癌新发病例约30.4万例,占女性全部恶性肿瘤发病的17.1%;死亡病例约7.0万例,占女性全部恶性肿瘤死亡的8.2%。近年来,随着我国人口老龄化的加速,工业化、城市化以及生活方式的改变,女性乳腺癌疾病负担日益加重。提高早期乳腺癌的检出率并进行及时有效的治疗是降低乳腺癌死亡率的有效措施。多个国家(如美国、德国、日本和澳大利亚等)已陆续开展人群乳腺癌筛查。我国现已开展包括乳腺癌筛查在内的多个国家重大公共卫生服务项目,如城市癌症早诊早治项目、全国农村妇女“两癌筛查”项目等,均取得了较好的社会效益。
美国医师协会、美国预防服务工作组(U.S. Preventive Services Task Force, USPSTF)、美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)、加拿大预防保健工作组等多个在世界上有影响力的学术组织和机构分别制定了各自的乳腺癌筛查指南,中国抗癌协会在2019年发布了《中国女性乳腺癌筛查指南》和《乳腺癌诊治指南与规范(2019年版)》。作为当前医疗实践中最常用的指导性文件,指南的发布与更新对提高应用决策的科学性和规范性发挥着重要的推动作用。高质量的指南是降低医疗成本和经济负担、改善医疗资源分布不均的有效工具,是规范医疗行为和提高医疗服务整体水平的重要手段。为实现对潜在乳腺癌患者的早发现、早诊断、早治疗,提高筛查的科学性、可行性和适用性,制定符合我国国情的乳腺癌筛查与早诊早治指南是十分重要和必要的。
鉴于此,受国家卫生健康委员会疾病预防控制局的委托和指导,国家癌症中心按照循证实践指南制定的方法和步骤,基于最新的研究证据,结合我国乳腺癌筛查实际情况,制定了《中国女性乳腺癌筛查与早诊早治指南(2021,北京)》(以下简称本指南)。
二、指南形成流程
本指南的设计与制定步骤参照世界卫生组织(World Health Organization, WHO)2014年发布的《世界卫生组织指南制定手册》,并根据国际实践指南报告规范(Reporting Items for Practice Guidelines in Healthcare, RIGHT)和指南研究与评价工具(AGREE Ⅱ)进行报告。
1. 指南发起机构与专家组成员:本指南由国家癌症中心发起。指南制定启动时间为2020年4月1日,定稿时间为2020年12月23日。
2. 指南工作组:本指南成立多学科工作组,主要涵盖肿瘤学、流行病学、超声学、乳腺内科、乳腺外科、放射治疗学、病理学、循证医学、卫生经济学、健康管理和政策研究等相关学科。证据的检索和评价由兰州大学和国家癌症中心合作完成。所有工作组成员均填写了利益声明表,与本指南不存在利益冲突。
3. 指南使用者与目标人群:本指南适用于各级医疗机构开展乳腺癌筛查工作。指南的使用者为各级医疗机构的医务工作者,包括影像科、乳腺外科等筛查相关学科医师及工作人员。指南推荐意见的应用目标人群为中国40岁及以上女性。
4. 临床问题的遴选和确定:本指南工作组通过系统查阅国内外乳腺癌筛查领域已发表的系统评价和指南,以及对全国28个省、自治区、直辖市各专业的95位临床医师开展第1轮问卷调研,初步拟定了30个临床问题。第2轮问卷调查邀请全国50位具有高级职称的临床医师对拟定临床问题进行重要性评价,并通过指南指导委员会会议,最终遴选出本指南拟解决的16个问题。
5. 证据的检索:指南制定工作组成立了证据检索与评价小组,针对最终纳入的关键临床问题,按照人群、干预、对照和结局原则对其进行中英文数据库检索。具体检索数据库包括PubMed、EMBASE、Cochrane Library、Web of Science、UpToDate、DynaMed、英国国家卫生与临床优化研究所(National Institute for Health and Care Excellence,NICE)、苏格兰校际指南网络、中国知网、万方数据库、维普资讯网、中国生物医学文献数据库和WHO临床试验注册平台,同时利用数据库的相似文献功能追踪乳腺癌筛查相关综述和系统评价/Meta分析的参考文献,继续补充检索。数据检索截止日期为2020年6月26日,检索策略见附件A。
6. 证据的评价与分级:证据检索与评价小组运用系统评价偏倚风险评价工具对纳入的系统评价、Meta分析进行偏倚风险评价。使用Cochrane Reviewer′s Handbook 5.0.1偏倚风险评价工具、诊断准确性研究的质量评价工具和纽卡斯尔-渥太华量表等对相应类型的原始研究进行偏倚风险评价。使用推荐意见分级的评估、制定及评价方法(Grading of Recommendations Assessment, Development and Evaluation, GRADE)对证据体进行分级,证据质量分级方法见表1。评价过程由两人独立完成,若存在分歧,则共同讨论或咨询第三方解决。

7. 推荐意见的形成:专家组针对基于证据检索与评价小组提供的临床问题进行系统评价,并基于证据给出推荐意见,同时考虑我国患者的偏好与价值观、干预措施的成本和利弊后,提出了符合我国筛查实践的推荐意见,分别于2020年9月10日和2020年10月10日进行2轮德尔菲推荐意见调查,共收集到166条反馈建议,于2020年11月13日进行面对面商议并于2020年12月进一步修改,形成了本指南的推荐意见。本指南中的推荐强度指在一定程度上能够相对明确推荐意见的利弊,其中强(1):当前证据能够相对明确提示干预措施利大于弊或弊大于利;弱(2):当前证据尚不足以明确筛查的利弊,或提示利弊相当(表1)。
8. 指南文稿的形成与外审:本指南工作组参考RIGHT报告规范草拟指南文稿,内部审议后形成征求意见稿。通过在国家癌症中心组织的会议等方式公开征求意见,并送期刊外审的形式收集修改意见,根据反馈结果完善形成最终稿。
9. 指南的传播、实施与更新:指南发布后,本指南工作组将主要通过以下方式对指南进行传播和推广:(1)在相关学术会议中对指南进行解读;(2)有计划地在中国部分省份组织指南推广专场会议,确保基层的恶性肿瘤筛查工作人员充分了解并正确应用本指南;(3)在学术期刊和书籍出版社公开发表本指南;(4)通过媒体等进行推广。指南工作组将综合临床实践需求与证据现状,并参考更新版指南报告清单,对本指南进行更新。计划每3年对本指南的推荐意见进行更新。
三、关键问题及推荐意见
(一)流行病学特征
问题1:我国女性乳腺癌发病率、死亡率和生存率情况
(A)我国女性乳腺癌负担重,是女性恶性肿瘤死亡的主要原因之一
(B)我国女性乳腺癌发病率呈上升趋势,并呈现出地区、年龄差异
(C)我国女性乳腺癌死亡率呈上升趋势,并呈现出地区、年龄差异
(D)我国女性乳腺癌5年相对生存率近年来有所升高
2020年中国女性乳腺癌发病率为59.0/10万,居全国女性恶性肿瘤发病谱首位。国家癌症中心公布的数据显示,2015年中国女性乳腺癌新发病例为30.4万例,占女性恶性肿瘤新发病例数的17.1%。不同地域女性乳腺癌发病率存在差异,总体为城市乳腺癌发病率(54.3/10万)高于农村(33.6/10万),女性乳腺癌发病率在城市和农村分别位列女性恶性肿瘤发病率首位和第2位。不同地区之间女性乳腺癌发病率也存在差异(东部>中部>西部),2015年中国东部地区女性新发乳腺癌14.6万例,发病率为57.4/10万;中部地区新发病例9.5万例,发病率为42.4/10万;西部地区新发病例6.3万例,发病率为32.7/10万,女性乳腺癌发病率分别位列东、中和西部地区女性恶性肿瘤发病的第1位、第1位和第2位。我国女性乳腺癌发病率呈上升趋势,2000—2014年各年份肿瘤登记地区的女性乳腺癌年龄别发病率分析结果显示,各年龄组女性乳腺癌发病率均有所上升,乳腺癌发病高峰年龄主要集中在50~59岁之间。
2020年中国女性乳腺癌死亡率为16.6/10万,居全国女性恶性肿瘤死亡谱第4位。根据国家癌症中心公布的数据显示,2015年中国女性乳腺癌死亡病例7.0万例。不同地域女性乳腺癌死亡率存在差异,总体城市女性乳腺癌死亡率(12.2/10万)高于农村(8.4/10万),女性乳腺癌死亡率在城市和农村分别位列女性恶性肿瘤死亡第3位和第6位。不同地区之间女性乳腺癌死亡率也存在差异,2015年中国东部地区女性乳腺癌死亡病例3.1万例,死亡率为12.0/10万;中部地区死亡病例2.4万例,死亡率为10.8/10万;西部地区死亡病例1.6万例,死亡率为8.2/10万,女性乳腺癌死亡率在东、中和西部地区分别位列女性恶性肿瘤死亡的第4位、第4位和第5位。我国女性乳腺癌死亡率呈上升趋势。乳腺癌年龄别死亡率随年龄的增长而上升,在85岁以上年龄组达到最高,国家癌症中心数据显示,2014年85岁以上年龄组女性乳腺癌死亡率高达52.8/10万。
2003—2015年全国17个肿瘤登记地区数据显示,女性乳腺癌5年合计相对生存率从73.1%(95% CI:71.2%~75.0%)增长至82.0%(95% CI:81.0%~83.0%);城市地区和农村地区2012—2015年女性乳腺癌5年相对生存率分别为84.9%和72.9%。
问题2:乳腺癌相关危险因素和保护因素
危险因素
(A)部分良性乳腺疾病患者的乳腺癌发生风险高
(B)子宫内膜异位症增加乳腺癌的发病风险
(C)高内源性雌激素水平会增加乳腺癌的发病风险
(D)特定的月经生育因素与乳腺癌发病相关
(E)乳腺癌家族史是乳腺癌的危险因素
(F)乳腺癌易感基因(breast cancer susceptibility genes, BRCA)1/2突变与乳腺癌发病相关
(G)肥胖是乳腺癌的危险因素
(H)大量饮酒是乳腺癌的危险因素
(I)吸烟是乳腺癌的危险因素
(J)暴露于治疗性电离辐射的女性乳腺癌发病风险增高
保护因素
(A)母乳喂养可以降低乳腺癌的发病风险
(B)适宜的体育锻炼可以降低乳腺癌的发病风险
1. 目前研究已明确的危险因素
(1)良性乳腺疾病:部分良性乳腺疾病(如乳腺囊肿和乳腺上皮不典型增生等)患者的乳腺癌发病风险增高。李红等对2002—2012年发表的良性乳腺疾病与乳腺癌关系的7项研究进行Meta分析,结果显示,良性乳腺疾病者患乳腺癌的风险为无良性乳腺疾病者的2.24倍(OR:2.24,95% CI:1.23~4.09)。戴琼等对1997—2007年发表的良性乳腺疾病与乳腺癌关系的31项研究(16 611例)进行Meta分析,结果显示,良性乳腺疾病者患乳腺癌的风险为无良性乳腺疾病者的1.95倍(OR:1.95,95% CI:1.59~2.38)。裴广军等对1996—2006年发表的良性乳腺疾病与乳腺癌关系的12项病例对照研究进行Meta分析,结果显示,良性乳腺疾病者患乳腺癌的风险为无良性乳腺疾病者的2.62倍(OR:2.62,95% CI:2.03~3.38)。
(2)子宫内膜异位症:子宫内膜异位症是乳腺癌的危险因素。Kvaskoff等对1993—2019年子宫内膜异位症和乳腺癌关系的20项研究进行Meta分析,结果显示,子宫内膜异位症者患乳腺癌的风险为无子宫内膜异位症者的1.04倍(RR:1.04,95% CI:1.00~1.09)。
(3)高内源性雌激素水平:无论是绝经前还是绝经后女性,高内源性雌激素水平均会增加乳腺癌的发病风险。Key等对18项前瞻性研究进行的Meta分析和Farhat等的研究表明,对于绝经后女性,激素水平上升与乳腺癌发病风险呈正相关。有学者汇总分析了7项前瞻性研究,共纳入767例绝经前乳腺癌女性和1 699例匹配对照者,结果显示,乳腺癌患病风险与雌二醇(OR:1.19,95% CI:1.06~1.35)、游离雌二醇(OR:1.17,95% CI:1.03~1.33)、雌激素酮(OR:1.27,95% CI:1.05~1.54)、雄烯二酮(OR:1.30,95% CI:1.10~1.55)、硫酸脱氢表雄酮(OR:1.17,95% CI:1.04~1.32)和睾酮(OR:1.18,95% CI:1.03~1.35)浓度呈正相关。
(4)月经生育因素:①初潮较早或绝经较晚:初潮年龄较早与乳腺癌发生风险较高有关。15岁或之后初潮的女性患雌激素受体和(或)孕激素受体阳性乳腺癌的风险低于13岁之前初潮的女性(HR:0.76,95% CI:0.68~0.85)。Cui等进行的一项基于美国人群的病例对照研究显示,初潮年龄≥14岁患乳腺癌的风险降低(OR:0.70,95% CI:0.55~0.88)。一项纳入117项研究的个体病例数据Meta分析结果显示,初潮每推迟1年,乳腺癌风险下降5%。此外,一项纳入了51篇文献的研究结果显示,在从未接受过激素治疗的人群中,绝经年龄每推迟1年,患乳腺癌的相对危险度增加3%(RR:1.03,95% CI:1.02~1.03)。②未经产与初次妊娠的年龄较高:未经产和初次妊娠较晚的女性患乳腺癌的风险增加。一项研究显示,未经产女性患乳腺癌的风险是经产女性的1.32倍(OR:1.32,95% CI:1.06~1.63)。在绝经期或接近绝经期的女性中,与未经产女性相比,首次生产年龄为20岁、25岁和35岁女性乳腺癌的累积发病率(直到70岁)分别降低20%、10%和升高5%。③流产:一篇针对有人工流产史中国女性的Meta分析共纳入36篇文献,结果显示,与没有人工流产史的女性相比,有人工流产的女性患乳腺癌的风险增加44%(OR:1.44,95% CI:1.29~1.59),对于人工流产达到2次或2次以上的女性,患乳腺癌风险分别增加76%和89%。
(5)乳腺癌家族史:Nindrea等对纳入的10项研究进行Meta分析,结果显示,有乳腺癌家族史人群患乳腺癌的风险为正常人群的3.34倍(OR:3.34,95% CI:2.68~4.15);Vishwakarma等对纳入的21 511例乳腺癌患者进行分析,结果显示,有乳腺癌家族史的人群乳腺癌发病风险为健康人群的5.33倍(OR:5.33,95% CI:2.89~9.82)。
(6)基因突变:BRCA增加乳腺癌发病风险。具有BRCA1/2致病性突变的患者发生乳腺癌、卵巢癌和其他恶性肿瘤的风险增加。对于BRCA1突变携带者,≤70岁时乳腺癌累积风险为55%~70%,BRCA2突变携带者的相应累积风险为45%~70%。此外,BRCA1突变携带者从成年早期到30~40岁时的乳腺癌发生率升高,BRCA2突变携带者从成年早期到40~50岁时的乳腺癌发生率升高,此后至80岁为平台期,乳腺癌发生率为20~30/1 000人年。与BRCA2突变携带者或BRCA1/2突变阴性者相比,BRCA1突变携带者更可能发生三阴性乳腺癌。Guo等在一项Meta分析中指出,BRCA1启动子高甲基化人群患乳腺癌的风险为一般人群的1.76倍(HR:1.76,95% CI:1.15~2.68)。
(7)肥胖:一项纳入了12项观察性研究的系统评价和Meta分析结果显示,在队列研究中脂肪含量最高的人群患乳腺癌风险为脂肪含量最低的人群的1.44倍(RR:1.44,95% CI:1.33~1.56)。世界癌症研究基金会(World Cancer Research Fund, WCRF)和美国癌症研究所(American Institute for Cancer Research, AICR)在2018年发布的癌症预防报告(第3版)中汇总了肥胖与绝经前或绝经后女性乳腺癌发病风险的相关证据,大量流行病学证据和剂量-反应关系分析支持同样的结论,即肥胖会增加绝经后女性乳腺癌的发病风险。
(8)生活方式因素:①饮酒:饮酒人群的乳腺癌发病风险增高。WCRF/AICR共纳入10项研究对绝经前乳腺癌发病风险进行剂量-反应Meta分析,结果显示,每天摄入10 g酒精可使乳腺癌发病风险增加5%(RR:1.05,95 %CI:1.02~1.08);对绝经后乳腺癌发病风险的剂量-反应Meta分析纳入22项研究,结果显示,每天摄入10 g酒精可使乳腺癌发病风险增加9%(RR:1.09,95% CI:1.07~1.12)。陶苹等对纳入的27项研究进行Meta分析,结果显示,有饮酒史人群患乳腺癌的风险为无饮酒史人群的1.16倍(OR:1.16,95% CI:1.01~1.32)。Bagnardi等对纳入的118项研究进行Meta分析,结果显示,重度饮酒人群患乳腺癌的风险为不饮酒和偶尔饮酒人群的1.61倍(RR:1.61,95% CI:1.33~1.94)。②吸烟:吸烟人群乳腺癌的发病风险增高。美国卫生与公众服务部于2014年系统汇总了吸烟与乳腺癌发病风险的相关证据,纳入22项队列研究和27项病例对照研究,结果显示,曾经吸烟使乳腺癌发病风险升高10%。吸烟时间长(20年或以上),每天吸烟量多(20支或以上),则使乳腺癌发病风险增加13%~16%。陶苹等对纳入的27项研究进行Meta分析,结果显示,有吸烟史人群患乳腺癌的风险为无吸烟史人群的1.50倍(OR:1.50,95% CI:1.03~2.20)。Gaudet等在美国癌症协会癌症预防研究的一项队列研究中发现,正在吸烟人群的乳腺癌发病率为非吸烟人群的1.24倍(HR:1.24,95% CI:1.07~1.42),有吸烟史人群的乳腺癌发病率为非吸烟人群的1.13倍(HR:1.13,95% CI:1.06~1.21)。
(9)暴露于治疗性电离辐射:暴露于治疗性电离辐射的女性患乳腺癌的风险增高。Ron的研究显示,行多次胸部透视检查的女性肺结核患者患乳腺癌的风险增加。年轻时胸部暴露于电离辐射如接受过放射治疗的霍奇金淋巴瘤的女性,其患乳腺癌的风险增加,且女童肿瘤患者接受高剂量放疗后乳腺癌标化发病率比为24.20(95% CI:20.70~28.30)。另一项研究显示,乳腺癌的发病风险随胸部放射剂量呈线性增加,与乳腺癌发病风险相关的电离辐射因素包括照射时的年龄、照射持续时间和辐射剂量等。
2. 目前研究已明确的保护因素
(1)母乳喂养:现有研究表明,母乳喂养可以降低乳腺癌的发病风险。一项评估母乳喂养对孕产妇健康结果影响的系统评价提示,12个月母乳喂养可使乳腺癌的患病风险降低26%(OR:0.74,95% CI:0.69~0.79),说明母乳喂养是乳腺癌的保护因素。与从不母乳喂养者相比,曾经母乳喂养者乳腺癌的患病风险下降22%(OR:0.78,95% CI:0.74~0.82),母乳喂养<6个月和母乳喂养6~12个月者乳腺癌的患病风险分别降低7%(OR:0.93,95% CI:0.88~0.99)和9%(OR:0.91,95% CI:0.87~0.96)。Victora等的研究显示,母乳喂养可以预防乳腺癌,将母乳喂养普及化后,每年可减少20 000名因乳腺癌死亡的患者。Shamshirian等的Meta分析结果显示,13~24个月的母乳喂养是乳腺癌的保护因素(OR:0.68,95% CI:0.46~0.90)。一项纳入24篇研究的Meta分析结果显示,累计母乳喂养较长时间,与乳腺癌的患病风险呈负相关(RR:0.47,95% CI:0.37~0.60)。
(2)体育锻炼:流行病学研究证据显示,适宜的体育锻炼可以降低女性乳腺癌的发病风险。WCRF/AICR在2018年发布的癌症预防报告(第3版)共纳入4项研究对体育锻炼和绝经前乳腺癌的发病风险进行Meta分析,结果显示,体育锻炼和绝经前乳腺癌的发病差异无统计学意义(RR:0.93,95% CI:0.79~1.08),体育锻炼对降低绝经前乳腺癌的发病风险证据有限。在体育锻炼对绝经后乳腺癌发病风险影响的Meta分析中,共纳入8项研究,结果显示,高水平体育锻炼可使绝经后乳腺癌的发病风险降低13%(RR:0.87,95% CI:0.79~0.96)。McTiernan等的研究显示,与缺乏体育锻炼的女性相比,定期进行体育锻炼的女性乳腺癌的发病风险降低14%(RR:0.86,95% CI:0.78~0.95)。2016年的一篇针对38项前瞻性研究的Meta分析提示,与缺乏体育锻炼的女性相比,积极进行体育锻炼的女性乳腺癌的发病风险下降12%(RR:0.88,95% CI:0.85~0.90)。
(二)结局和定义
问题3:筛查相关的乳腺癌病理分型和TNM分期
(A)乳腺癌的组织学分型包括:(1)非浸润性癌:导管原位癌、小叶原位癌;(2)浸润性癌:浸润性癌非特殊型、浸润性小叶癌、小管癌、黏液癌等
(B)根据美国癌症联合会(American Joint Committee on Cancer, AJCC)TNM分期系统(第8版),乳腺癌分为0期、Ⅰ期、Ⅱ期、Ⅲ期和Ⅳ期
乳腺癌的组织学分型推荐采用WHO乳腺肿瘤分类标准(2019年版)。
乳腺癌分期系统推荐应用AJCC第8版(表2)。细化定义如下。
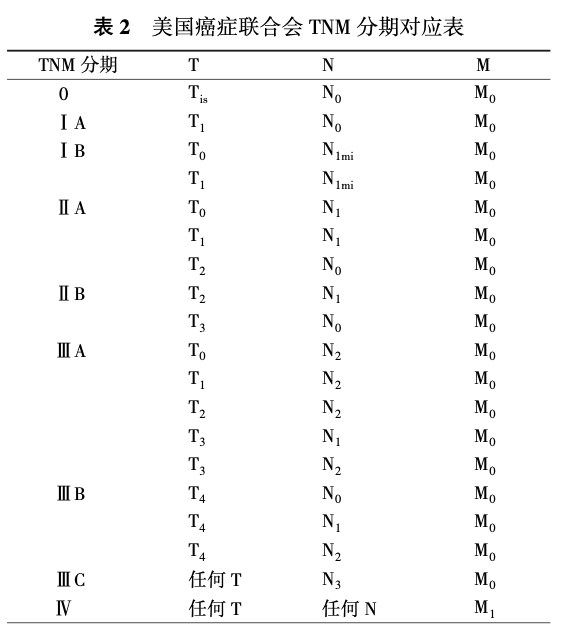
(1)原发性肿瘤(T):TX:原发性肿瘤无法评估;T0:无原发性肿瘤证据;Tis:原位癌;T1:肿瘤最大径≤20 mm;T2:肿瘤最大径>20 mm但≤50 mm;T3:肿瘤最大径>50 mm;T4:肿瘤直接侵袭胸壁和(或)皮肤(溃疡或肉眼可见的皮肤结节),不论大小。
(2)区域淋巴结(N):pNX:区域淋巴结无法评估(先前已切除,或未切除进行病理学检查);pN0:无区域淋巴结转移证据;pN1mi:微转移(单枚淋巴结单张肿瘤切片中,肿瘤最大径>0.2 mm和(或)多于200个细胞,但≤2.0 mm);pN1a:1~3枚腋窝淋巴结转移,至少1枚转移灶>2.0 mm;pN1b:在没有腋窝淋巴结转移的情况下,同侧内乳前哨淋巴结转移,且转移灶>0.2 mm,孤立的肿瘤细胞群除外;pN1c:同时出现pN1a和pN1b;pN2:4~9枚腋窝淋巴结转移,或影像学检查显示同侧内乳淋巴结转移而无腋窝淋巴结转移;pN3:10枚或更多腋窝淋巴结转移(至少1枚转移灶>2.0 mm);或锁骨下淋巴结(属第Ⅲ水平腋窝淋巴结)转移(pN3a);或影像学检查显示同侧内乳淋巴结转移,伴1枚或多枚Ⅰ、Ⅱ级腋窝淋巴结转移;或3枚以上腋窝淋巴结转移,以及前哨淋巴结活检证实但临床未发现的内乳淋巴结微转移灶或宏转移灶(pN3b);或同侧锁骨上淋巴结转移(pN3c)。
(3)远处转移(M):M0:没有远处转移的临床或放射影像学证据;M1:临床和放射影像学方法确定和(或)组织学证实存在>0.2 mm的远处转移灶。
问题4:乳腺早期癌和癌前病变定义
(A)乳腺早期癌指肿瘤直径<2 cm,同侧腋窝淋巴结未见转移,且无远处转移
(B)乳腺癌前病变包括小叶肿瘤(不典型小叶增生)、柱状细胞病变(扁平上皮不典型增生)和导管上皮不典型增生
早期乳腺癌和癌前病变定义主要参考来源包括WHO乳腺肿瘤分类(2019年版)、中国女性乳腺癌筛查指南和中国抗癌协会乳腺癌诊治指南与规范(2019年版)等多部国内外指南和专家共识。
问题5:筛查的危害
(A)筛查的危害是指与未筛查相比,个人或群体在参与筛查过程中产生的任何负面效应
(B)过度诊断是指发现一种病变,即便它没有被诊断,也不会导致疾病发病率或死亡率的增加。假阳性是指根据筛查结果而推荐进行后续其他诊断性检查(包括进一步的影像学检查或组织取样检查),但在其后1年内未查出乳腺癌的情况;以及部分被诊断的恶性肿瘤,即使未接受临床治疗,终生也不会死于该恶性肿瘤的情况
(C)假阳性结果导致的压力:筛查个体得到假阳性结果后,由于压力导致产生的焦虑、抑郁、沮丧等负面情绪
(D)其他:乳腺X线检查所带来的躯体不适或疼痛导致人群筛查依从性降低
(E)假阴性漏诊导致的负面效应
乳腺癌筛查的危害主要参考UpToDate数据库《乳腺癌筛查的策略与推荐》、《乳腺癌筛查:效果和危害的证据以及NCCN和USPSTF发布的乳腺癌筛查指南。具体包括以下。
(1)筛查的危害:乳腺癌筛查的危害包括过度诊断、假阳性结果、患者焦虑和不必要的治疗及其风险。乳腺癌筛查最严重的危害是过度诊断、假阳性结果。
(2)过度诊断:筛查的过度诊断是指通过筛查手段发现的早期恶性肿瘤患者,其中部分恶性肿瘤并不会继续生长、转移并导致患者死亡。这些患者如果不通过筛查发现,就不会在临床上出现有重要意义的疾病诊断。过度诊断会导致不必要的检查和治疗,以及恶性肿瘤诊断和治疗的心理负担和其他后果。在所有诊断为乳腺癌的女性中,过度诊断率从≤10%到>50%不等。这些差异可能来源于研究设计不同,比如各研究纳入的研究对象不同(如是否纳入乳腺导管内原位癌、纳入研究的年龄段)、使用的测量和估算的方法不同等。过度诊断使某些患者接受了针对恶性肿瘤的治疗,但恶性肿瘤未被发现也不会造成伤害,从而使得筛查既带来不利影响(躯体和心理)也未降低死亡率。
(3)假阳性结果:增加假阳性风险的因素包括:年轻、乳腺密度高、乳腺癌家族史或个人史、既往乳腺活检、正在使用雌激素、较短的筛查间隔、未与之前检查结果对比以及放射科医师个人的过度解读倾向。假阳性结果在较年轻女性中更常见,因为这类人群中乳腺X线摄影的特异性较低。此外,因为乳腺癌常规筛查推荐每年或隔年进行复查,所以假阳性风险