1、IMpassion031研究的最终分析(摘要号:LBA1)原标题:Final analysis of the placebo-controlled randomised phase 3 IMpassion031 trial evaluating neoadjuvant atezolizumab (atezo) plus chemotherapy (CT) followed by open-label adjuvant atezo in patients (pts) with early-stage triple-negative breast cancer (eTNBC)推荐理由:针对早期三阴性乳腺癌(TNBC)患者,在新辅助化疗的基础上联合阿替利珠单抗能提高pCR率。IMpassion031研究的最终分析,能明确该治疗方案的长期获益。魔方补充:IMpassion031是一项多中心,随机,双盲的III期临床试验,旨在评估阿替利珠单抗联合化疗在早期TNBC新辅助治疗中的疗效和安全性。研究共入组333例患者,1:1随机分为阿替利珠单抗+化疗组或安慰剂+化疗组。主要研究终点是在意向治疗(ITT)人群和PD-L1阳性人群中评估pCR,次要终点包括OS、无事件生存期(EFS)、无病生存期(DFS)和生活质量。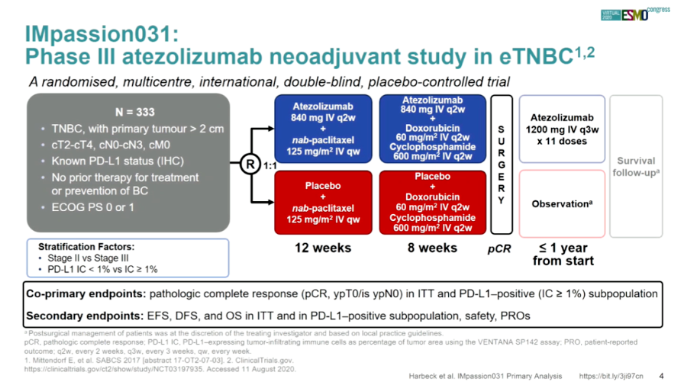
2020年10月,Lancet发表了IMpassion031研究的期中结果,与安慰剂+化疗组相比,阿替利珠单抗+化疗组能显著改善ITT人群的pCR(57.6% vs 41.1%,P=0.0044)(下图)。
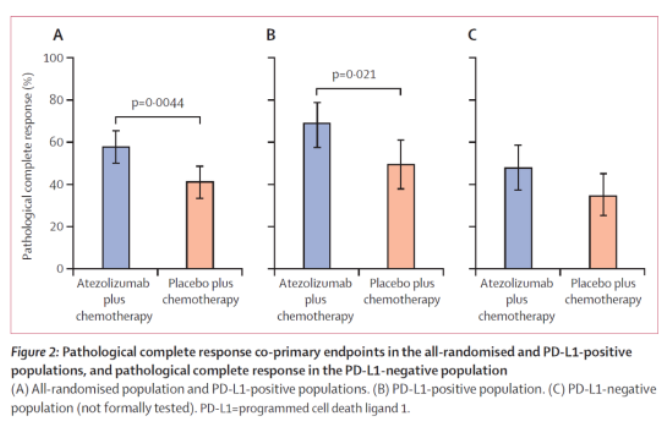
2022年9月,NPJ Breast Cancer发表了IMpassion031研究的PRO结果,在新辅助治疗期间,两组在各评估指标方面均相似。辅助治疗期间,两组中大多数症状值与基线时相似,但疲乏除外,其保持高于基线水平,且在阿替利珠单抗+化疗组中更为明显。2、ICARUS-BREAST01研究结果(摘要号:189O)原标题:A phase 2 Study of Patritumab Deruxtecan (HER3-DXd), in patients (pts) with advanced breast cancer (ABC), with biomarker analysis to characterize response to therapy (ICARUS-BREAST01) 推荐理由:在ASCO 2022年会期间公布的I/II期试验数据提示,HER3-DXd在乳腺癌所有亚型中均显示出积极的数据(下图),且不十分依赖于HER3表达水平。通过ICARUS-BREAST01研究,能否进一步证明有意义的生物标记物,能帮助预测药物疗效或耐药?
3、HER2DX的pCR预测meta分析(摘要号:126MO)原标题:HER2DX and pathological complete response in HER2-positive breast cancer: a combined analysis of 4 neoadjuvant studies推荐理由:HER2DX基因检测正成为HER2阳性早期乳腺癌有前景的生物标志物,该meta分析纳入4项新辅助治疗研究,分析HER2DX在预测pCR中的作用。4、SOLTI TOT-HER3 Part B(摘要号:124O)原标题:Patritumab deruxtecan (HER3-DXd) in hormonal receptor-positive/HER2-negative (HR+/HER2-) and triple negative breast cancer (TNBC): results of part B of SOLTI TOT-HER3 window of opportunity trial推荐理由:ESMO BC 2022会议期间公布了SOLTI TOT-HER3 Part A数据,HER3-DXd新辅助治疗显示出有前景的抗肿瘤活性。而这种活性是否与激素受体表达水平相关?魔方补充:SOLTI-1805 TOT-HER3研究,是一项机会窗(window-of-opportunity)、多中心、术前试验,旨在评估单剂量HER3-DXd在多个乳腺癌队列中的抗肿瘤活性。纳入绝经前/绝经后妇女,或未经治疗的男性患者,原发性可手术早期乳腺癌(超声/MRI≥1 cm)以及局部Ki67≥10%。Part A部分:纳入78名患者,根据基线ERBB3 mRNA水平进行分类。患者接受单剂量HER3-DXd(6.4 mg/kg)。Part B部分:包括两个队列。第一个队列招募20名HR+/HER2-早期乳腺癌患者,第二个队列招募15名TNBC患者。患者将接受单剂量HER3-DXd(5.6 mg/kg)。检测治疗前后(C1D21,即第1周期第21天)活检和血液样本。Part A部分的主要目的是评估治疗前后,肿瘤样本之间CelTIL(肿瘤细胞及浸润淋巴细胞)评分的平均变化。总体试验人群和Part B部分的次要目标包括:配对肿瘤样本之间CelTIL评分的变化,C1D21的总缓解率,CelTIL变化与ERBB3和HER3 IHC基线表达的相关性,ERBB3和HER3的动态变化,PAM50各亚型CelTIL的变化,安全性以及其他药代动力学、基因组学和循环生物标志物。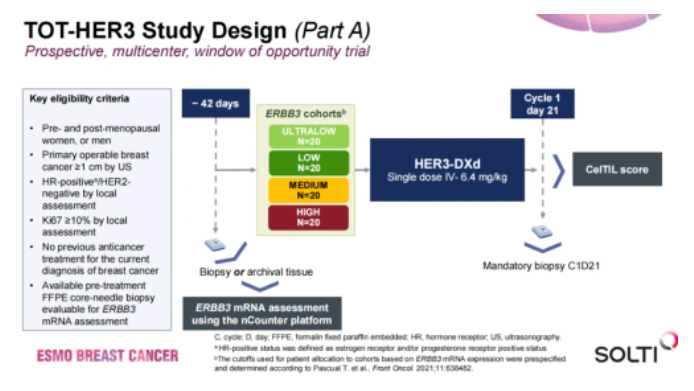
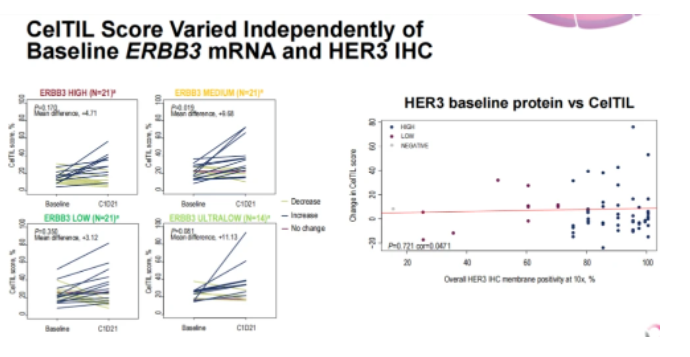
2022 ESMO BC期间公布了Part A部分的数据,在入组的78例患者中,77例达到了可评估主要终点。根据治疗前ERBB3 mRNA水平,将患者分为高(n=21)、中(n=21)、低(n=21)和超低(n=14)四组。PAM50亚型:Luminal(Lum)A型占52%,Luminal B型占41%,HER2过表达占3%,Basal-like占4%。总体ORR为45%,CelTIL在C1D21时显著升高,但这种增加趋势仅在出现缓解的患者中观察到,在病情稳定的患者中未显示出。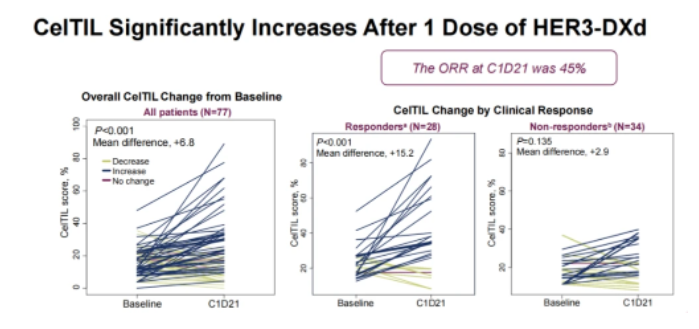
非Luminal亚型和高复发风险评分与CelTIL的高反应相关。治疗前ERBB3 mRNA水平与CelTIL的变化或临床应答无关,治疗后配对Ki67显著降低(p<0.001),而ERBB3 mRNA未出现显著降低。在C1D21时,患者免疫基因被诱导,增殖基因被抑制。CelTIL评分独立于基线ERBB3 mRNA和HER3免疫组水平。安全性方面,74例(95%)患者报告了任何级别的不良事件。
5、TNBC伴有残留病灶患者的ctDNA检测(摘要号:95MO)原标题:Circulating tumor DNA (ctDNA) dynamics in patients (pts) receiving capecitabine (CAPE) for early-stage triple-negative breast cancer (eTNBC) with an incomplete response to neoadjuvant therapy (NAT)推荐理由:针对那些接受新辅助治疗后未达到完全缓解的早期TNBC患者,接受卡培他滨治疗是否有助于清除ctDNA?6、CAPItello-291研究的亚组分析(摘要号:187O)原标题:Capivasertib and fulvestrant for patients (pts) with aromatase inhibitor (AI)-resistant HR+/HER2- advanced breast cancer (ABC): subgroup analyses from the Phase 3 CAPItello-291 trial推荐理由:针对HR+转移性乳腺癌,在氟维司群的基础上联合capivasertib可以改善PFS,尤其是存在PI3KCA/AKT/PTEN改变的患者中。来看亚组数据,尤其是没有上述信号通路改变的患者。
魔方补充:CAPItello-291研究是一项全球、多中心、双盲、随机的III期临床试验,共纳入708例患者,旨在评估capivasertib+氟维司群对比安慰剂+氟维司群治疗HR+/HER2-晚期乳腺癌患者的疗效和安全性,这些患者在接受AI治疗期间或之后疾病复发或进展。研究允许患者既往接受过CDK4/6抑制剂治疗(至少51%),但既往未接受过SERD、mTOR抑制剂、PI3K抑制剂或AKT抑制剂。
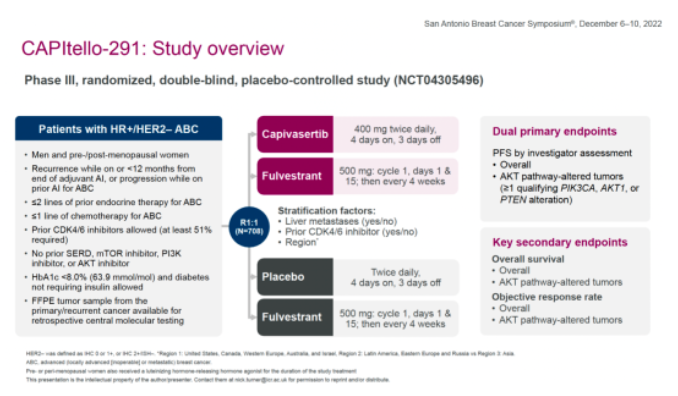
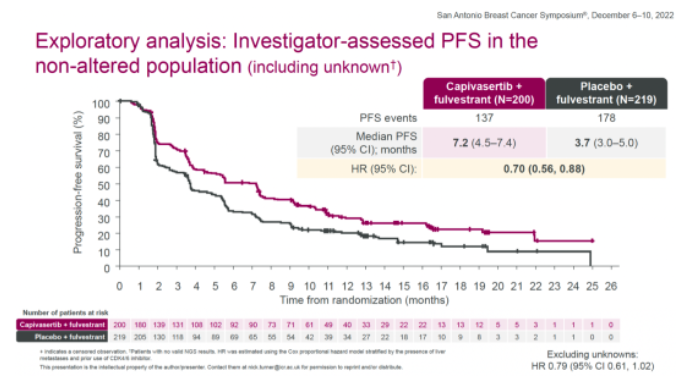
研究的主要终点:研究者评估的总体人群和存在AKT信号通路改变人群的PFS。关键次要终点:总体人群和AKT信号通路改变人群的OS以及ORR。分层因素包括是否肝转移、是否接受过CDK4/6抑制剂治疗和地区。患者基线特征方面,总体人群中,~69%的患者既往接受过CDK4/6抑制剂治疗。capivasertib+氟维司群组和安慰剂+氟维司群组中,分别有43.7%(155/355)和38.0%(134/353)的患者存在任何形式的AKT信号通路改变。2022年SABCS期间公布了主要终点方面,在全体人群中,capivasertib+氟维司群组和安慰剂+氟维司群组的中位PFS分别为7.2个月和3.6个月,HR=0.60(0.51-0.71,two-sided P<0.001)。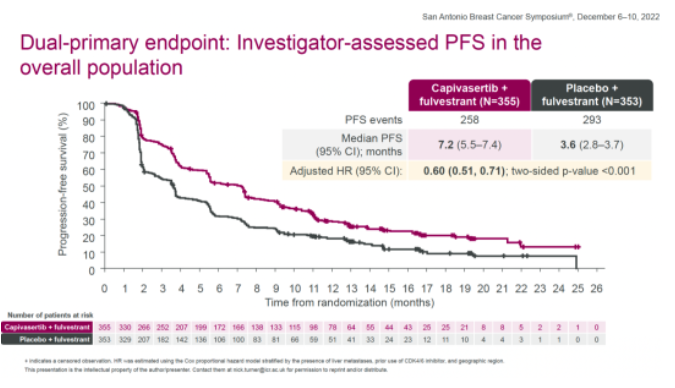
在AKT通路改变人群中,capivasertib+氟维司群组和安慰剂+氟维司群组的中位PFS分别为7.3个月和3.1个月,HR=0.50(0.38-0.65,two-sided P<0.001)。
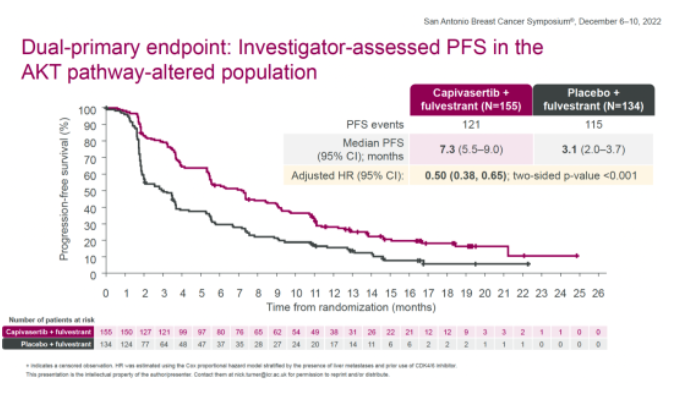
探索性分析显示,在AKT通路未改变人群中(包括状态未知),两组的中位PFS分别为7.2个月和3.7个月,HR=0.70(0.56-0.88)。
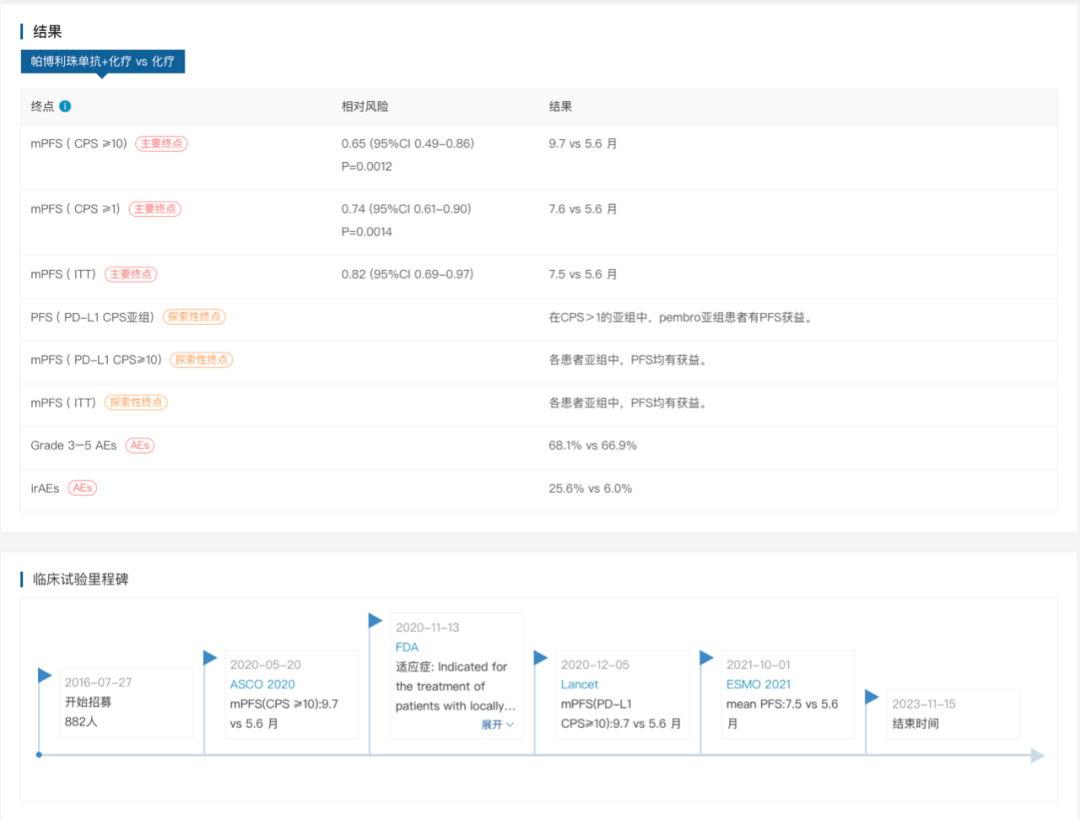
ORR方面,全体人群中capivasertib+氟维司群组和安慰剂+氟维司群组的ORR分别为22.9%和12.2%;AKT通路改变人群中,两组的ORR分别为28.8%和9.7%。OS数据尚未成熟。7、KN355中不良反应和预后之间的关系(摘要号:191MO)原标题:KEYNOTE-355: Outcomes in patients who discontinued chemotherapy before pembrolizumab and in patients with immune-mediated AEs.推荐理由:多个肿瘤类型的数据提示不良反应和免疫治疗药物的有效性可能具有相关性。同样也要寻找早期停止化疗这部分患者和预后之间是否存在相关性。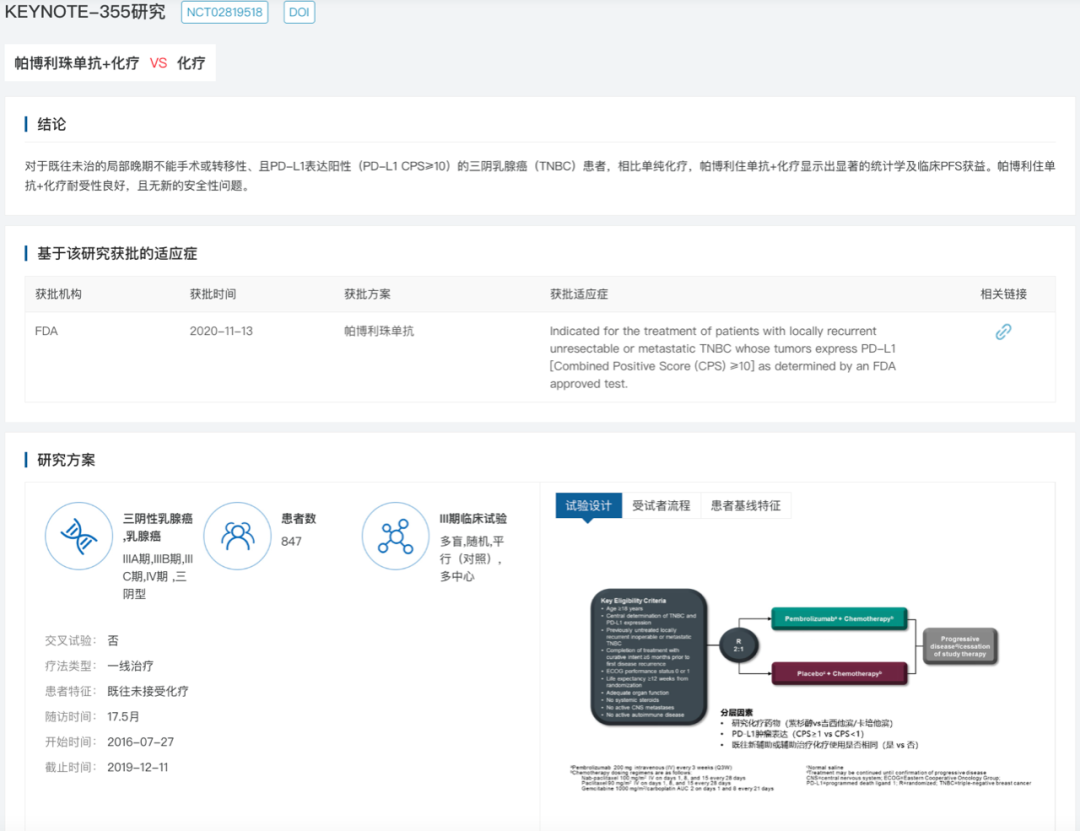
8、DESTINY-Breast 04研究中ER-low(IHC 0~10%)患者的预后(摘要号:192MO)原标题:DESTINY-Breast04 subgroup analyses of trastuzumab deruxtecan (T-DXd) vs treatment of physician’s choice (TPC) in patients (pts) with human epidermal growth factor 2 (HER2)-low, estrogen-receptor (ER) expression immunohistochemistry (IHC) 0-10% metastatic breast cancer (mBC) 推荐理由:在HER2-low转移性乳腺癌患者中,T-DXd已经成为一种新的治疗选择。这项研究或可回答在ER-low患者中的疑问,ER-low正在成为HR阳性和TNBC之间的边界。魔方补充:雌激素受体(ER)作为乳腺癌的生物学标志物,影响着乳腺癌的治疗选择。美国临床肿瘤学会和美国病理学家学会(ASCO/CAP)指南(2010年)将ER≥1%定为ER阳性,ER<1%定为ER阴性。ASCO/CAP指南(2020年)中,新增ER在1%~10%定为ER低表达,ER>10%定为ER高表达。ER低表达乳腺癌,作为一种特定表达形式,其生物学特征与ER阴性相似。ER阳性乳腺癌中,ER低表达患者占2%~5% 。针对HER-2、CDK4/6、PIK3CA等靶点的药物可以改善这部分患者的预后,但证据尚不充分。
9、KN119研究中的基因表达谱分析(摘要号:190MO)原标题:Association of 18-Gene Expression Profile (GEP) With Clinical Outcomes in Patients With Metastatic Triple-Negative Breast Cancer (mTNBC) Treated With Pembrolizumab (Pembro) or Chemotherapy (Chemo) in KEYNOTE-119推荐理由:KEYNOTE-119研究显示,在TNBC二线或以上治疗,帕博利珠单抗单药与化疗相比未能改善预后。能否从肿瘤生物学和免疫特征上探索一个亚组患者,能从免疫治疗中获益?10、EMERALD(elacestrant,摘要号:188O),DB02(T-DXd,摘要号:186O),monarchE(阿贝西利,摘要号:93MO),ABCSG 22注册研究(摘要号:260MO)的患者报告结局(PRO)推荐理由:了解新型抗肿瘤药物对患者生存质量的影响非常重要。



















